 25 de abril de 1900, en Zúrich (Suiza) – 15 de diciembre de 1958, en Zúrich (Suiza)
25 de abril de 1900, en Zúrich (Suiza) – 15 de diciembre de 1958, en Zúrich (Suiza)
Wolfgang Ernest Paulí, se licenció en Física en el Döblinger Gymnasium de Viena (Austria) en 1918 y, tan solo dos meses después, publicó su primer artículo sobre la teoría de la relatividad general de Albert Einstein. En 1921, logró el doctorado en Física en la Universidad de Múnich (Alemania), tutelado por Arnold Sommerfeld, un físico alemán especializado en los estudios del átomo.
A sugerencia de éste, publicó una monografía de 237 páginas sobre la relatividad en la revista alemana Encyklopaedie der mathematischen Wissenschaften (“Enciclopedia de ciencias matemáticas”), recibiendo elogios de Einstein y que, actualmente, sigue siendo una de las referencias básicas sobre el tema.
Estuvo un año en la Universidad de Göttingen (Alemania) como asistente de Max Born, aprendiendo todos los secretos del a Mecánica Cuántica, rama de la Física contemporánea en la que Born era una autoridad mundial. Un año más tarde, se trasladó al Instituto de Física Teórica en Copenhague (Dinamarca) para colaborar con Niels Bohr, otro referente de la Física que marcó profundamente la carrera de Pauli.
Entre 1923 y 1928, ejerció como profesor de Física Teórica en Universidad de Hamburgo. Es durante esta época cuando desarrolló su famoso Principio de Exclusión y su otra teoría no relativista del Espín.
En 1928, dejó Alemania para ocupar la Cátedra de Física Teórica del Instituto Tecnológico Federal (ETH) de Zúrich (Suiza).
En 1931 y 1935, se trasladó a Estados Unidos para impartir algunos seminarios en la Universidad de Michigan y en el Instituto de Estudios Avanzados de Princeton, respectivamente.
En este periodo de tiempo, en 1932, Pauli realizó su tercera gran aportación a la ciencia, la propuesta teórica de la existencia del neutrino, una partícula subatómica que podía ofrecer una explicación satisfactoria al decaimiento beta del radio (aunque no fue detectada experimentalmente hasta 1956).
En 1933, publicó “Los principios fundamentales de la Mecánica cuántica”, considerado uno de los textos fundamentales de dicha materia.
En 1938, Hitler anexionó Austria por lo que se convirtió en ciudadano alemán a la fuerza. Tras el estallido de la Segunda Guerra Mundial se traslada a Estados Unidos para hacerse cargo de la cátedra de Física en Princeton.
En 1945, recibe el Premio Nobel de Física por su descubrimiento del Principio de Exclusión y, un año más tarde, recibe la nacionalidad estadounidense.
Finalizada la guerra, regresa a Zurich hasta su muerte con 58 años.
El spin
 En los inicios, la teoría cuántica reconocía la existencia de tres números cuánticos: le principal (que, según Niels Bohr, define la energía del electrón en su órbita), el magnético (que marca la orientación de la órbita en el espacio) y el acimutal (que describe la forma de la órbita elíptica).
En los inicios, la teoría cuántica reconocía la existencia de tres números cuánticos: le principal (que, según Niels Bohr, define la energía del electrón en su órbita), el magnético (que marca la orientación de la órbita en el espacio) y el acimutal (que describe la forma de la órbita elíptica).
La Física tradicional aceptaba la existencia de estos números, pero recelaba de la Mecánica Cuántica porque, con ellos, era imposible explicar el espectro del átomo.
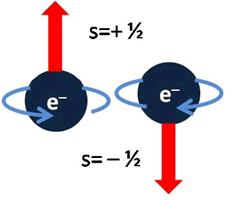
Para resolver este problema, en 1924, Pauli añadió un cuarto número, el spin, que representaba la medida del momento angular del electrón o de su dirección de giro sobre sí mismo y estableció los dos únicos valores que puede tomar: ½ y – ½.
Principio de exclusión de Pauli
En 1925, Pauli enunció este principio en virtud del cual no puede haber, en un mismo átomo, dos electrones con idéntico valor para los cuatro números cuánticos. Por lo tanto, los electrones, partículas con carga eléctrica que se mueven alrededor del núcleo atómico, se excluyen mutuamente (ya que no pueden solaparse uno con otro en la misma órbita porque se repelen).
El espacio dentro de un átomo en el que se encuentran los electrones y no puede permanecer al mismo tiempo si no son enteros y tienen la misma disposición se llama orbital.
Gracias a este principio, se pudo explicar la ordenación de los elementos en la tabla periódica, así como establecer las órbitas de sus electrones. Después se descubrió que también se podía aplicar a todas las partículas elementales englobadas dentro del grupo de los fermiones (aquellas cuyo giro no es un número entero).
El neutrino
 Se había detectado un fenómeno de difícil explicación, la denominada desintegración beta. Era una discrepancia de momentos y energías que se traducía en la emisión o expulsión de electrones por parte del núcleo atómico. Lo extraño es que, en su propia naturaleza, contradecía el principio de conservación de la energía.
Se había detectado un fenómeno de difícil explicación, la denominada desintegración beta. Era una discrepancia de momentos y energías que se traducía en la emisión o expulsión de electrones por parte del núcleo atómico. Lo extraño es que, en su propia naturaleza, contradecía el principio de conservación de la energía.
Pauli hizo una propuesta teórica sobre este fenómeno en la que indicaba la existencia de una partícula neutra sumamente ligera, no detectada experimentalmente hasta ese momento, cuya emisión coincidía con la del electrón. Dicha partícula, surgía en el momento de la desintegración beta, llevándose la energía y el momento que faltaban; pero al poseer una masa nula o prácticamente nula, apenas interaccionaba con la materia por lo que resultaba muy complicado de detectar.
El físico italiano Enrico Fermi, apoyó esta teoría bautizando la partícula con el nombre de neutrino y, en 1956, Frederick Reines logró detectarla experimentalmente dando una plena validez a la especulación teórica de Pauli. Posteriormente, científicos como Lederman, Schwaartz y Steinberger pusieron de manifiesto la existencia de varios tipos de neutrinos.
¿Qué es el efecto Pauli?
En España conocido como el “efecto demo”, se refiere a las aparentemente misteriosas averías de los equipos técnicos en presencia de determinadas personas. Esto le ocurría a Pauli, por eso, se le puso su nombre. Sin embargo, Wolfgang Ernest Pauli, consciente de su reputación, no se sintió ofendido y le resultaba bastante gracioso cada vez que se manifestaba este efecto (que no hay que confundir con el tipo de fenómeno físico que es su Principio de Exclusión).
 25 de abril de 1900, en Zúrich (Suiza) – 15 de diciembre de 1958, en Zúrich (Suiza)
25 de abril de 1900, en Zúrich (Suiza) – 15 de diciembre de 1958, en Zúrich (Suiza) En los inicios, la teoría cuántica reconocía la existencia de tres números cuánticos: le principal (que, según Niels Bohr, define la energía del electrón en su órbita), el magnético (que marca la orientación de la órbita en el espacio) y el acimutal (que describe la forma de la órbita elíptica).
En los inicios, la teoría cuántica reconocía la existencia de tres números cuánticos: le principal (que, según Niels Bohr, define la energía del electrón en su órbita), el magnético (que marca la orientación de la órbita en el espacio) y el acimutal (que describe la forma de la órbita elíptica). Se había detectado un fenómeno de difícil explicación, la denominada desintegración beta. Era una discrepancia de momentos y energías que se traducía en la emisión o expulsión de electrones por parte del núcleo atómico. Lo extraño es que, en su propia naturaleza, contradecía el principio de conservación de la energía.
Se había detectado un fenómeno de difícil explicación, la denominada desintegración beta. Era una discrepancia de momentos y energías que se traducía en la emisión o expulsión de electrones por parte del núcleo atómico. Lo extraño es que, en su propia naturaleza, contradecía el principio de conservación de la energía.
